1 前言
電鍍、石化和制藥是當(dāng)今全球三大污染工業(yè)。就我國電鍍廢水而言,據(jù)不完全統(tǒng)計,全國電鍍廠點約1萬家,職工約有40萬人,每年排出的電鍍廢水約40億m3[1]。1999年,全國工業(yè)和城市生活廢水排放總量為401億m3,其中工業(yè)廢水排放量197億m3[2]。由此可見,電鍍廢水的排放量約占廢水總排放量的10%,占工業(yè)廢水排放量的20%。電鍍廢水不僅量大,而且對環(huán)境造成的污染也嚴(yán)重,因為電鍍廢水中不僅含有氰化物等劇毒成分,而且含有Cr、Zn、Cu、Ni等自然界不能降解的重金屬離子。因此對電鍍廢水的治理歷來受到各國政府的重視,對電鍍廢水各種治理方法和工藝的研究也很多,其中主要有化學(xué)沉淀法、電解法、離子交換法和膜處理法等,化學(xué)法是目前國內(nèi)外應(yīng)用最多的,而且隨著pH-ORP自動控制儀的使用,化學(xué)法處理電鍍廢水有逐漸增加的趨勢。就上海來說[3],廢水處理中化學(xué)法所占比例由80年代中期的55.2%增至1990年的66.1%,再增至90年代中期的80.1%;而國外采用化學(xué)法的比例更是高達80%~90%[4]。
然而化學(xué)法處理電鍍廢水雖然具有技術(shù)成熟、投資小、費用低、適應(yīng)性強、自動化程度高等諸多優(yōu)點,但其缺點也是顯而易見的:首先,化學(xué)法會產(chǎn)生大量的污泥難以處理;另外,由于化學(xué)法要向水中加入大量化學(xué)藥劑,使出水的含鹽量高,難以回用,如果出水外排不僅有可能造成二次污染,還浪費了寶貴的水資源。
電鍍污泥的處置及二次污染
電鍍污泥是化學(xué)法處理電鍍廢水的最大缺陷。由于電鍍廢水自身就含有Cr、Zn、Cu、Ni等重金屬離子,在處理過程中又加入次氯酸鈉、硫化鈉、硫酸亞鐵、氫氧化鈉或氫氧化鈣等各種化學(xué)藥劑,因此沉淀的電鍍污泥成分很復(fù)雜,這給電鍍污泥的處理和利用帶來困難。對電鍍污泥的處置,目前國內(nèi)外還沒有特別有效的方法,國外大都采用填埋或固化處理。在我國,電鍍污泥部分被送至磚廠燒磚,部分與煤混合燃燒后混入爐渣,而有些企業(yè)則將電鍍污泥隨意露天堆放[3,5-9]。這些簡單的處理方法都有可能造成污泥的二次污染。
2.1 露天堆放造成二次污染
污泥的主要污染成份是Cr(OH)3,當(dāng)棄露于空氣中,在堿性條件下,能被空氣中的O2氧化,使Cr3+可逆性地轉(zhuǎn)變成Cr6+。反應(yīng)方程為:
4Cr(OH)3+3O2+8OH-=4Cr+10H2O (1)
在常溫(25℃)下,該反應(yīng)的自發(fā)性由化學(xué)自由能決定。根據(jù)公式:
反應(yīng)自發(fā)進行。實驗測定結(jié)果也證實暴露在空氣中的含鉻污泥可與O2反應(yīng)生成六價鉻。因此電鍍污泥若不加處理而任意棄置,受到風(fēng)吹雨淋,會四溢漂流,致使污染擴散,給環(huán)境帶來嚴(yán)重后果[10]。
2.2 混入粘土中燒磚造成污泥的二次污染
電鍍污泥中的鉻、鐵主要以氫氧化物的形態(tài)存在,即Cr(OH)3、Fe(OH)3和Fe(OH)2,在燒制過程中,當(dāng)溫度達到200℃時,這些物質(zhì)就會發(fā)生分解生成各自的氧化物,反應(yīng)如下:
2Cr(OH)3=Cr2O3+3H2O (2)
Fe(OH)2=FeO+H2O (3)
2Fe(OH)3=Fe2O3+3H20 (4)
上述反應(yīng)隨溫度的升高而加劇,所以在燒磚過程中,電鍍污泥中的鉻、鐵主要以氧化物形態(tài)存在。在更高溫度下,鉻的氧化物形態(tài)發(fā)生變化:
2Cr2O3+3O2=4CrO3 (5)
此時,Cr3+被氧化為Cr6+。在電鍍污泥形成過程中,摻入大量NaOH或Ca(OH)2,而一般粘土中含有石英、長石及碳酸鹽等,當(dāng)把電鍍污泥與粘土一起混合燒磚時。其物相組成以及焙燒條件與鉻酸鹽工業(yè)很相似,可能發(fā)生生成鉻酸鈉的反應(yīng),使三價鉻氧化為六價鉻[11]。
2.3 摻入煤中焚燒入渣造成六價鉻污染
將污泥拌入煤中燃燒,則在鍋爐高溫(1200℃)條件下,污泥中Cr(OH)3變成Cr2O3,同時,Cr3+受到高溫活化,無形中加速了與O2的反應(yīng):
2Cr2O3+3O2=4CrO3
根據(jù)化學(xué)熱力學(xué)公式:
由此可見,該反應(yīng)為吸熱反應(yīng),高溫下的反應(yīng)速度會大大加快,污泥中的Cr3+轉(zhuǎn)化為Cr6+進入爐渣。如果這些爐渣被用來鋪路或被建材行業(yè)利用,將會對環(huán)境和人體健康帶來不可想象的危害[10]。
3 處理后的出水外排造成的二次污染
3.1 活性氯對水體造成二次污染
在用堿性氯化法處理含氰廢水時,常用的氯氧化劑主要有次氯酸鈉、次氯酸鈣和液氯等,有時由于加入的氯氧化劑過量,造成最終出水中含有少量的活性氯。通常,活性氯含量達0.002mg/L時就會對水生動植物產(chǎn)生毒害作用[12]。
3.2 重金屬對水體造成二次污染
由于不同重金屬離子沉淀的最佳pH值不同,如果在電鍍廢水的處理過程中,最終溶液的pH值偏離某金屬氫氧化物最小溶解度pH點,則有可能造成該金屬離子沉淀不完全或沉淀后反溶,從而使出水中某些重金屬離子的含量過高,對水體造成污染。
3.3 Cr3+氧化為Cr6+對水體或土壤造成二次污染
對于鉻來說,國家規(guī)定的排放標(biāo)準(zhǔn)為:[Cr6+]<0.5mg/L,[總鉻]<1.5mg/L,由于在排放的廢水中有可能含有因沉淀不完全而溶解的Cr3+,這部分Cr3+在一定條件下會被重新氧化為Cr6+而污染環(huán)境,即:
4Cr(OH)3+3O2+8OH-=4Cr+10H2O (6)
當(dāng)排出的廢水進入地下或滲入土壤后,由于土壤環(huán)境的不同,對鉻的氧化或還原能力亦不同[13],如果土壤中的有機物含量低而錳氧化物含量高,則Cr3+被氧化為Cr6+的趨勢將大于Cr6+被還原為Cr3+的趨勢,因此在這樣的土壤環(huán)境中,Cr3+就有可能被氧化為Cr6+而重新污染環(huán)境。
盡管目前對水中Cr3+被氧化為Cr6+的機理尚有爭議,但在水中Cr3+被氧化為Cr6+而對環(huán)境可能造成污染這一點上,人們的認(rèn)識是一致的。
有研究表明[14],當(dāng)Fe3+存在時,Cr3+有可能通過光誘導(dǎo)氧化(Light-Induced Oxida-tion)生成Cr6+具體反應(yīng)如下:
Fe3++OH-+hv→Fe2++·OH (7)
·OH+Cr3+→Cr4++OH- (8)
·OH+Cr4+→Cr5++OH- (9)
·OH+Cr5+→Cr6++OH- (10)
將(7)(8)(9)(10)相加得:
3Fe3++Cr3++hv→3Fe2++Cr6+ (11)
此外,亦有人認(rèn)為[15],錳氧化物Mn(Ⅲ、Ⅳ)的存在也能導(dǎo)致Cr3+氧化為Cr6+,總的反應(yīng)方程為:
2Cr3++3MnO2+2H2O=2HCr+3Mn2++2H+ (12)
由此可見,在電鍍廢水的治理中,不能僅僅考慮到廢水的達標(biāo)排放;對于電鍍污泥以及出水的合理處置和利用,也是關(guān)系到整個廢水處理工程成敗與否的關(guān)鍵一環(huán),兩者應(yīng)放在同等重要的位置
電鍍廢水處理過程中的二次污染
現(xiàn)有網(wǎng)友評論 0 條 進入論壇
4 應(yīng)采取的措施
對于化學(xué)法處理電鍍廢水所存在的污泥以及處理后出水外排有可能造成的二次污染問題,通常采用以下的治理措施:
4.1 合理選擇藥劑,嚴(yán)格控制加藥量
用次氯酸鈉代替漂白粉可以減少氧化破氰時產(chǎn)生的污泥量。傳統(tǒng)的化學(xué)沉淀還原法一般單獨使用亞鐵鹽還原Cr6+,這將導(dǎo)致產(chǎn)生大量的Fe(OH)3沉淀,從而導(dǎo)致污泥量過大;若采用先加Na2S還原,再用亞鐵鹽還原沉淀工藝,則還原徹底且沉淀污泥量少。
4.2 改進工藝流程
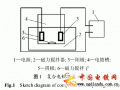
為了使氧化還原反應(yīng)完全或沉淀完全,往往要向廢水中投加過量的氧化劑(如次氯酸鈉)和還原劑(如硫化鈉或硫酸亞鐵),這不僅造成藥劑上的浪費,而且還會增加污泥量以及出水的含鹽量。如果將化學(xué)法和其他處理方法(如電滲析)聯(lián)合使用,組成如下的工藝流程:
則不但能夠節(jié)約藥劑、減少污泥量,而且化學(xué)法處理后的上清液經(jīng)電滲析處理后,淡水可以達到回用標(biāo)準(zhǔn),實現(xiàn)電鍍廢水的閉路循環(huán),既不污染環(huán)境,又充分利用了水資源。 4.3 污泥的資源化或無害化處理 由于電鍍廢水水質(zhì)、選用化學(xué)藥劑的不同,導(dǎo)致電鍍污泥的組成復(fù)雜且多變,從而給電鍍污泥的處置和利用造成困難。電鍍污泥的資源化目前大都還處于實驗室研究階段,因為經(jīng)濟上無利可圖,污泥的資源化還很難在工業(yè)上應(yīng)用。電鍍污泥的無害化處理也同樣面臨經(jīng)濟上的困難。因此對于污泥的處理,一方面需要探索更經(jīng)濟有效的處理方法,更重要的還是需要企業(yè)對環(huán)保的重視以及政府和環(huán)保部門的行政干預(yù)。