電鍍?cè)?/strong>包含四個(gè)方面:電鍍液、電鍍反應(yīng)、電極與反應(yīng)原理、金屬的電沉積過(guò)程。
首先電鍍液有六個(gè)要素:主鹽、絡(luò)合劑、附加鹽、緩沖劑、陽(yáng)極活化劑和添加劑。
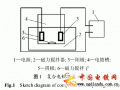
電鍍反應(yīng)中的電化學(xué)反應(yīng):下圖是電鍍裝置示意圖,被鍍的零件為陰極,與直流電源的負(fù)極相連,金屬陽(yáng)極與直流電源的正極聯(lián)結(jié),陽(yáng)極與陰均浸入鍍液中。當(dāng)在陰陽(yáng)兩極間施加一定電位時(shí),則在陰極發(fā)生如下反應(yīng):從鍍液內(nèi)部擴(kuò)散到電極和鍍液界面的金屬離子Mn+從陰極上獲得n個(gè)電子,還原成金屬M(fèi)。另一方面,在陽(yáng)極則發(fā)生與陰極完全相反的反應(yīng),即陽(yáng)極界面上發(fā)生金屬M(fèi)的溶解,釋放n個(gè)電子生成金屬離子M n+。

電鍍?cè)硌b置示意圖
電極及反應(yīng)機(jī)理
A、電極電位
當(dāng)金屬電極浸入含有該金屬離子的溶液中時(shí),存在如下的平衡,即金屬失電子而溶解于溶液的反應(yīng)和金屬離子得電子而析出金屬的逆反應(yīng)應(yīng)同時(shí)存在:Mn++ne = M
平衡電位與金屬的本性和溶液的溫度﹐濃度有關(guān)。為了精確比較物質(zhì)本性對(duì)平衡電位的影響﹐人們規(guī)定當(dāng)溶液溫度為250C﹐金屬離子的濃度為1mol/L時(shí)﹐測(cè)得的電位叫標(biāo)準(zhǔn)電極電位。標(biāo)準(zhǔn)電極電位負(fù)值較大的金屬都易失掉電子被氧化﹐而標(biāo)準(zhǔn)電極電位正值較大的金屬都易得到電子被還原。
B、極化
所謂極化就是指有電流通過(guò)電極時(shí)﹐電極電位偏離平衡電極電位的現(xiàn)象。所以﹐又把電流-電位曲線(xiàn)稱(chēng)為極化曲線(xiàn)。產(chǎn)生極化作用的原因主要是電化學(xué)極化和濃差極化。
(1)電化學(xué)極化
由于陰極上電化學(xué)反應(yīng)速度小于外電源供給電子的速度﹐從而使電極電位向負(fù)的方向移動(dòng)而引起的極化作用。
(2)濃差極化
由于鄰近電極表液層的濃度與溶液主體的濃度發(fā)生差異而產(chǎn)生的極化稱(chēng)濃差極化﹐這是由于溶液中離子擴(kuò)散速度小于電子運(yùn)動(dòng)造成的。
電鍍過(guò)程是鍍液中的金屬離子在外電場(chǎng)的作用下,經(jīng)電極反應(yīng)還原成金屬原子并在陰極上進(jìn)行金屬沉積的過(guò)程。
電鍍?cè)砗?jiǎn)單而言,就是在含有欲鍍金屬的鹽類(lèi)溶液中,以被鍍基體金屬為陰極,通過(guò)電解作用,使鍍液中欲鍍金屬的陽(yáng)離子在基體金屬表面沉積出來(lái),形成鍍層。