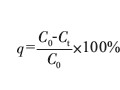1 了解水的重要意義
水是電鍍液的主要組分,電鍍幾乎都是在水溶液中進(jìn)行的。盡管有非水溶液電鍍的報(bào)道(如在甘油中鍍鋁,在二甲基亞砜中鍍納米半導(dǎo)體線,在乙酰胺–尿素–溴化鉀熔體中鍍半導(dǎo)體納米合金),但均限于實(shí)驗(yàn)室研究,并無工業(yè)化應(yīng)用。溶液由溶質(zhì)和溶劑組成。電鍍液是一種水溶液,即以水為溶劑,溶質(zhì)則是鍍液中其它可溶于水的組分。離開了水就配不出電鍍液。
水與電鍍的重要工藝條件pH密切相關(guān)。不了解水的電離特性就不知道pH的來歷,也就無法理解為什么要控制這一重要的工藝條件,也無法理解鍍層燒焦這一重要故障的實(shí)質(zhì)。
水的電解現(xiàn)象是不少電鍍問題的根源。電解除油為什么比化學(xué)除油快且徹底?為什么有陰極、陽極電解除油之分?陰極電流效率為什么有高有低?工件為什么會(huì)產(chǎn)生針孔、麻點(diǎn)?為什么陽極面積較小、陽極電流密度過大時(shí)陽極會(huì)不導(dǎo)電而鈍化? 為什么鋼鐵件可以采用電解方法使其從無氰堿銅液中 由鈍化態(tài)轉(zhuǎn)為活化態(tài)才有好的結(jié)合力?這些問題都與 水的電解現(xiàn)象密切相關(guān)。
2 水分子的特性
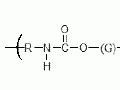
無機(jī)化合物可分為氧化物、酸、堿、鹽等幾大類。物質(zhì)由分子組成,分子又由原子組成,原子之間由“鍵”相連。水實(shí)際上是氫的氧化物。氫的氧化物中常見的有 2 種:一種是由 1 個(gè)氧原子與 2個(gè)氫原子組成的普通水分子H2O,另一種是電鍍中常用的雙氧水H2O2(又稱過氧化氫),由 2個(gè)氫原子和 2個(gè)氧原子構(gòu)成。雙氧水不穩(wěn)定,易分解成氧氣和水,具有氧化性,電鍍中常被用于氧化無機(jī)或有機(jī)雜質(zhì)。其最大優(yōu)點(diǎn)是生成的水是鍍液組分,無副作用。
水分子中 3個(gè)原子不是排在一條直線上,2個(gè)氫氧鍵之間有104°40′的夾角。由于這一夾角的存在,分子中正負(fù)電荷的“重心”不重合:水分子中靠近氧原子的一端帶負(fù)電性,靠近氫原子的一端帶正電性,使水分子成為“極性分子”。電鍍書刊中常講到“電極電位”,水分子的極性正是產(chǎn)生電位的重要原因。
3 水的離子積與 pH
在溶液中,分子能電離成正、負(fù)離子的物質(zhì)稱為電解質(zhì)。幾乎百分之百電離的稱為強(qiáng)電解質(zhì),如鍍液中加入的大多數(shù)酸、堿、鹽類;僅部分電離而還有部分以分子形式存在的稱為弱電解質(zhì),如硼酸、醋酸;幾乎不電離而主要以分子形式存在的稱為非電解質(zhì),如甘油、三乙醇胺、聚乙二醇等。而作為溶劑的水,本身也是一種弱電解質(zhì),只有很少一部分電離為氫離子(帶正一價(jià),用 H+表示)和氫氧根離子(帶負(fù)一價(jià),用 OH–表示): H O U H+ + OH− 。化學(xué)上用“ U ”表示“可逆反應(yīng)”,即反應(yīng)既可以向右進(jìn)行(稱為正反應(yīng)),也可以向左進(jìn)行(稱為逆反應(yīng))。
溶液酸堿性對(duì)電鍍效果影響很大,任何搞電鍍的人都必須對(duì)pH 的來歷及其含義有非常明確的認(rèn)識(shí)。
4 水的電解
既然任何情況下水溶液中都必然存在或多或少的氫離子 H+與氫氧根離子 OH–,那么在通電時(shí)帶正電荷的氫離子H+也可能在陰極表面獲得1個(gè)電子而還原(化學(xué)上將得到電子、化合價(jià)降低的反應(yīng)稱為還原反應(yīng))為氫原子(稱為活性氫原子,具有很強(qiáng)的還原能 力),化合價(jià)由正一價(jià)降為零價(jià);2個(gè)活性氫原子再結(jié)合成1個(gè)氫氣分子(以氣體形式逸出)。用 e–表示電子,則上述還原反應(yīng)可表示為:
H+ + e– → H , 2H → H2 ↑
(化學(xué)反應(yīng)式中,“↑”表示氣體,“↓”表示沉淀) 即 2H+ + 2e– → H2 ↑ (1) 同樣,帶負(fù)電荷的 OH–也可能在陽極上失去1個(gè)電子而被氧化(化學(xué)上稱失去電子、化合價(jià)上升的反應(yīng)為氧化反應(yīng)),反應(yīng)式為:OH– – e– → OH , 4OH → 2H2O + O2 ↑ 即 4OH–– 4e–→ 2H2O + O2 ↑ (2)
合并(1)式與(2)式,即為水的電解反應(yīng)。通電時(shí),在陽極上可能產(chǎn)生氧氣,在陰極上可能產(chǎn)生氫氣。電解除油的實(shí)質(zhì)就是水的電解反應(yīng)。
5 水的純度問題
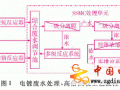
自然界中現(xiàn)成的水總含有礦物質(zhì)等雜質(zhì)。例如,地下水中或多或少地溶有鈣、鎂等雜質(zhì);被污染了的水則雜質(zhì)更多,更復(fù)雜。含鈣、鎂量大的水稱為“硬水”,若用于鋅酸鹽鍍鋅,則會(huì)影響鍍層質(zhì)量。基本去除了鈣、鎂雜質(zhì)的水稱為“軟水”,其去除過程稱為水的“軟化處理”。水中的鈣、鎂雜質(zhì)經(jīng)加熱或干燥后會(huì)生成水垢。鍋爐中火管上沉積的過厚水垢不但影響導(dǎo)熱性,而且水垢突然開裂時(shí)可能引發(fā)鍋爐爆炸,故鍋爐用水應(yīng)先經(jīng)軟化處理,而且應(yīng)定期停爐除垢。裝飾鍍鉻、光亮鍍銀、鍍錫件若用硬水清洗后直接烘干,生成的水垢會(huì)使工件表面發(fā)花,故要求高的產(chǎn)品鍍后要用純水清洗。水中的其它雜質(zhì)對(duì)電鍍也多有害處。如含氯離子多的水,用于光亮酸銅鍍前清洗,會(huì)向酸銅液引入過多的氯離子而引起故障;用于塑料鍍前處理的銀鹽活化或鍍鋅后的銀鹽黑鈍化配液或其處 理前清洗,氯離子 Cl–會(huì)與銀離子 Ag+生成難溶的氯化銀AgCl 沉淀而使溶液失效報(bào)廢。經(jīng)處理后的電鍍廢水(稱為中水)也含有較多鹽分與有機(jī)雜質(zhì)。中水只能回用于要求不高的鍍前酸洗或化學(xué)除油等工序,而不 能回用于鍍前清洗。要回用于要求高的鍍前清洗,必須經(jīng)活性炭處理、離子交換處理、反滲透或電滲析的 深度再處理,去除水中有害的有機(jī)雜質(zhì)和多種陰、陽離子雜質(zhì)后才行。將水加熱為蒸汽再冷凝后得到的水,稱為蒸餾水,其中雜質(zhì)相對(duì)較少。用現(xiàn)代膜分離技術(shù)或離子交換法除去了H+、OH–以外的其它陰、陽離子的水稱為去離子水,其電導(dǎo)率越低則純度越高。