【簡介】
王春霞,趙晴,杜楠,簡志超
(南昌航空大學(xué)材料科學(xué)與工程學(xué)院,江西南昌330063)
[摘要]無氰硫代硫酸鹽鍍銀液的穩(wěn)定性對(duì)其生產(chǎn)應(yīng)用影響很大。采用陳化和連續(xù)鍍試驗(yàn)測(cè)試了無氰硫代硫酸鹽鍍銀液的穩(wěn)定性,并從理論上分析了鍍液不穩(wěn)定的原因,提出了有效維持鍍液穩(wěn)定的方法。結(jié)果表明:鍍液在低溫避光環(huán)境中可長期保存;及時(shí)補(bǔ)充鍍液中硫代硫酸鹽和焦亞硫酸鉀的含量,連續(xù)鍍15 d后鍍液仍澄清,無黑色沉淀。
[關(guān)鍵詞]鍍液穩(wěn)定性;檢測(cè)分析;鍍液陳化;連續(xù)鍍;無氰硫代硫酸鹽鍍銀液
[中圖分類號(hào)]TQ153.1+6[文獻(xiàn)標(biāo)識(shí)碼]B[文章編號(hào)]1001-1560(2011)02-0067-03
0·前言
無氰硫代硫酸鹽鍍銀層具有優(yōu)良的耐蝕性和可焊性,對(duì)人體無害且裝飾性好,近年來使用較多。新配制的無氰硫代硫酸鹽鍍液使用一段時(shí)間后,槽液易發(fā)黑,鍍層光澤度變差,光亮電流密度范圍變窄,操作極為不便,并且生產(chǎn)成本增加。加入穩(wěn)定劑改善鍍液穩(wěn)定性的效果不明顯,還會(huì)使鍍層質(zhì)量尤其是鍍層耐變色性和導(dǎo)電性變差。本工作采用陳化和連續(xù)鍍?cè)囼?yàn)測(cè)試硫代硫酸鹽鍍銀液的穩(wěn)定性,并從理論上分析了鍍液不穩(wěn)定的原因,提出了有效維護(hù)鍍液穩(wěn)定的方法。
1·試驗(yàn)
1.1標(biāo)準(zhǔn)無氰硫代硫酸鹽鍍銀液配方
50 g/L硝酸銀,200 g/L硫代硫酸銨,50 g/L焦亞硫酸鉀,pH值為5~6。
1.2鍍液穩(wěn)定性測(cè)試
1.2.1陳化試驗(yàn)
配制2份200 mL標(biāo)準(zhǔn)鍍液置于2個(gè)250 mL燒杯中,分別放置在室溫避光處和室外陽光下,每隔2~3 d分析1次,記錄鍍液中各成分含量的變化,每天只補(bǔ)加去離子水使鍍液保持在200 mL。另配制1份200 mL標(biāo)準(zhǔn)鍍液于250 mL燒杯中,置于40℃水浴恒溫槽中,每隔8~18 h分析1次,記錄鍍液各成分含量的變化,每天只補(bǔ)加去離子水使鍍液保持在200 mL。
1.2.2連續(xù)鍍?cè)囼?yàn)
配制2份200 mL標(biāo)準(zhǔn)鍍液置于2個(gè)250 mL燒杯中,室溫下白天通電8~9 h后斷電靜放過夜15~16 h,每隔2~3 d分析1次,記錄鍍液中各成分含量的變化,補(bǔ)加其中一份標(biāo)準(zhǔn)鍍液各成分至初始濃度,而另一份每天只補(bǔ)加去離子水使鍍液保持在200 mL。
1.3鍍液成分分析
1.3.1指示劑的配制
鐵銨釩:將2 g硫酸高鐵銨溶于100 mL沸水中,滴加煮沸過的濃硝酸直到棕色褪去。
淀粉:將1 g可溶性淀粉以少量水調(diào)成漿倒入100mL沸水中,攪勻,沸騰1~2 min,冷卻,加入2~5滴氯仿。
1.3.2主鹽硝酸銀的測(cè)定
用移液管吸取5 mL待測(cè)液置于250 mL錐形瓶中,在通風(fēng)櫥內(nèi)加濃硝酸、濃硫酸各10 mL,加熱到冒白煙,待黃色沉淀全部溶解后自然冷卻至室溫,加30~40mL水搖勻,繼續(xù)冷卻,加2~3滴鐵銨釩指示劑,用0.1mol/L標(biāo)準(zhǔn)硫氰酸銨溶液滴定至淺紅色剛剛出現(xiàn)時(shí)為終點(diǎn)。計(jì)算公式如下:
ρ=(C×V1×M)/V2
式中ρ———硝酸銀含量,g/L
C———標(biāo)準(zhǔn)硫氰酸銨溶液的摩爾濃度,0.1 mol/L
V1———消耗標(biāo)準(zhǔn)硫氰酸銨溶液的體積,L
M———硝酸銀的摩爾質(zhì)量,169.87 g/mol
V2———待測(cè)液體積,0.005 L
1.3.3配位劑硫代硫酸鈉的測(cè)定
用移液管吸取1 mL待測(cè)液放入250 mL錐形瓶中,加5 mL 40%的甲醛和25 mL水,搖勻,放置15min,加淀粉指示劑1 mL,用0.1 mol/L標(biāo)準(zhǔn)碘溶液滴定至呈現(xiàn)藍(lán)色0.5 min不消失為終點(diǎn)。計(jì)算公式如下:
ρ=2(C×V1×M)/V2
式中ρ———硫代硫酸鈉含量,g/L
C———標(biāo)準(zhǔn)碘溶液的摩爾濃度,0.1 mol/L
V1———消耗碘溶液的體積,L
M———硫代硫酸鈉的摩爾質(zhì)量,158.2 g/mol
V2———待測(cè)液體積,0.001 L
1.3.4穩(wěn)定劑焦亞硫酸鉀的測(cè)定
用移液管吸取1 mL待測(cè)液放入250 mL錐形瓶中,加蒸餾水25 mL、淀粉1 mL,用0.1 mol/L標(biāo)準(zhǔn)碘溶液滴定至呈現(xiàn)藍(lán)色不消失為終點(diǎn)。計(jì)算公式如下:
ρ=2[C×(V1-V2)×M]/V3
式中ρ———焦亞硫酸鉀含量,g/L
C———標(biāo)準(zhǔn)碘溶液的摩爾濃度,0.1 mol/L
V1———滴定配位劑和穩(wěn)定劑所消耗的碘的體積,L V2———滴定配位劑所消耗的碘的體積,L
M———焦亞硫酸鉀的摩爾質(zhì)量,55.6 g/mol
V3———待測(cè)液體積,0.001 L
2·結(jié)果與討論
2.1陳化
鍍液暴露于陽光下時(shí)各成分含量隨時(shí)間的變化見表1。

從表1可以看出:隨放置時(shí)間延長,鍍液中各成分含量都逐漸減少,且配位劑、穩(wěn)定劑含量變化非常大。結(jié)果顯示:1 d后鍍液完全發(fā)黑,10 d后完全分層,下層為黑色沉淀物,上層為清澈的鍍液。鍍液在室溫避光處靜置時(shí)各成分含量隨時(shí)間的變化見表2。

由表2可知:隨放置時(shí)間延長,鍍液的配位劑、穩(wěn)定劑含量變化較小。鍍液在室溫避光處放置時(shí)不發(fā)黑,不渾濁。
鍍液在40℃靜置時(shí)各成分含量隨時(shí)間的變化見表3。從表3可知:隨時(shí)間延長,鍍液中各成分含量都逐漸減少,26 h后配位劑、穩(wěn)定劑含量減少較大。26 h后鍍液開始發(fā)黑,70 h后鍍液完全發(fā)黑。

綜上所述,影響鍍液穩(wěn)定性的外界環(huán)境主要是陽光,其次是溫度,且鍍液發(fā)黑與鍍液中的配位劑和穩(wěn)定劑的含量有密切關(guān)系。
2.2連續(xù)鍍
連續(xù)鍍狀態(tài)下只補(bǔ)加去離子水、不補(bǔ)加鍍液成分時(shí)鍍液各成分含量隨時(shí)間的變化見表4。

從表4可知:隨時(shí)間延長各成分含量雖減少,但其比例比較恒定,說明鍍液成分含量減少主要是因?yàn)殡娀瘜W(xué)沉積;7 d后鍍液中配位劑、穩(wěn)定劑的含量非常低,也說明鍍液發(fā)黑與鍍液中的配位劑和穩(wěn)定劑有必然關(guān)系。在連續(xù)鍍狀態(tài)下,鍍液不會(huì)完全發(fā)黑,但7 d后有少許的黑色沉淀物,15 d后有大量的黑色沉淀物,且鍍層開始發(fā)花,有條紋出現(xiàn)。
連續(xù)鍍狀態(tài)下每天補(bǔ)加鍍液主要成分使其保持在初始濃度,15 d后鍍液仍清澈透明,且鍍層始終結(jié)晶細(xì)致、光滑。因此,在生產(chǎn)過程中要定期分析、補(bǔ)加鍍液成分。
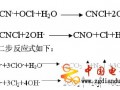
2.3鍍液黑色產(chǎn)物成因
硫代硫酸鹽鍍銀液長期在陽光下放置或連續(xù)生產(chǎn)而不及時(shí)補(bǔ)充鍍液各成分時(shí),槽液變黑、變渾而不夠穩(wěn)定,有如下2個(gè)主要原因[1]:



3·結(jié)論
(1)鍍液長期在陽光下或高溫下放置,槽液底部有黑色殘?jiān)e円和S脮r(shí)應(yīng)放置于避光、低溫環(huán)境中。
(2)鍍液長期生產(chǎn)而不及時(shí)補(bǔ)充配位劑、穩(wěn)定劑,鍍液會(huì)變渾,且底部有黑色殘?jiān)Ia(chǎn)時(shí)需定期分析、補(bǔ)充鍍液成分。
[參考文獻(xiàn)]
[1]鄒堅(jiān).硫代硫酸鹽鍍銀槽發(fā)黑故障的排除[J].電鍍與精飾,1995,17(3):30~31.
[2]陳壽椿.重要無機(jī)化學(xué)反應(yīng)(第2版)[M].上海:上海科技出版社,1982:29~53.[編校:鄭霞]